Tormenta de citoquinas y COVID-19
lunes , 20 de abril de 2020

Tormenta de citoquinas y COVID-19
A finales de diciembre de 2019, la Organización Mundial de la Salud (OMS) fue informada, por parte de las autoridades sanitarias de Wuhan (China), de 27 casos de neumonía, de etiología desconocida, en pacientes que tenían en común el haber estado en un mercado de mayoristas de animales vivos. El agente causal fue identificado posteriormente como un virus de la familia Coronavidae, desconocido hasta entonces, y al que se denominó SARS-CoV-2; el cuadro clínico asociado se denomina COVID-19. Desde esa primera notificación, los casos no han dejado de multiplicarse, lo que hizo que el 11 de marzo la OMS declarara esta infección como pandemia mundial. Los casos notificados han alcanzado más de 2 millones en todo el mundo y en España más de 180.000.
Seguir leyendo
La gravedad de esta infección radica en la gran capacidad de contagio de este virus y, sobre todo, la gravedad con la que se manifiesta la enfermedad en algunos pacientes, que ha dado lugar a más de 145.000 muertes. La tasa de mortalidad asociada a la infección por este virus es todavía desconocida, al no disponer exactamente del número real de infectados; recientemente, el director de la OMS ha advertido que esta tasa puede ser diez veces superior a la de la gripe. Aunque la mayoría de los pacientes presenta una sintomatología leve o moderada, algunos desarrollan una neumonía grave con insuficiencia respiratoria aguda o síndrome de distres respiratorio del adulto y fallo multiorgánico, que eventualmente puede llevarlos a la muerte. Ello ha llevado a la saturación de los sistemas sanitarios y a la parálisis social y económica mundial.
El esfuerzo de la comunidad médica y científica está dando lugar a una gran cantidad de información acerca de esta pandemia, como ha recogido la doctora Avendaño en un artículo publicado recientemente en Anales de la RANF (1). Esta información se modifica continuamente con nuevas evidencias sobre epidemiologia, características microbiológicas y clínicas del virus y las posibilidades de tratamiento farmacológico, mientras se obtiene una vacuna eficaz. Aunque existen numerosos ensayos clínicos en marcha, no disponemos por el momento de evidencias procedentes de ensayos controlados, que permitan recomendar un tratamiento específico para SARS-CoV-2. Algunos de los fármacos que se están utilizando son medicamentos ya autorizados para otras indicaciones, pero que todavía no han demostrado una eficacia científicamente probada para esta enfermedad. El Ministerio de Sanidad y Consumo de nuestro país actualiza continuamente un protocolo científico-técnico de manejo del coronavirus Covid-19 (2). En la última versión se incluye la participación del sistema inmunitario en la gravedad de la infección por SARS-CoV-2, lo que abre la posibilidad de encontrar un tratamiento eficaz para los casos más graves, centrado en dicha participación.
Citoquinas y COVID-19
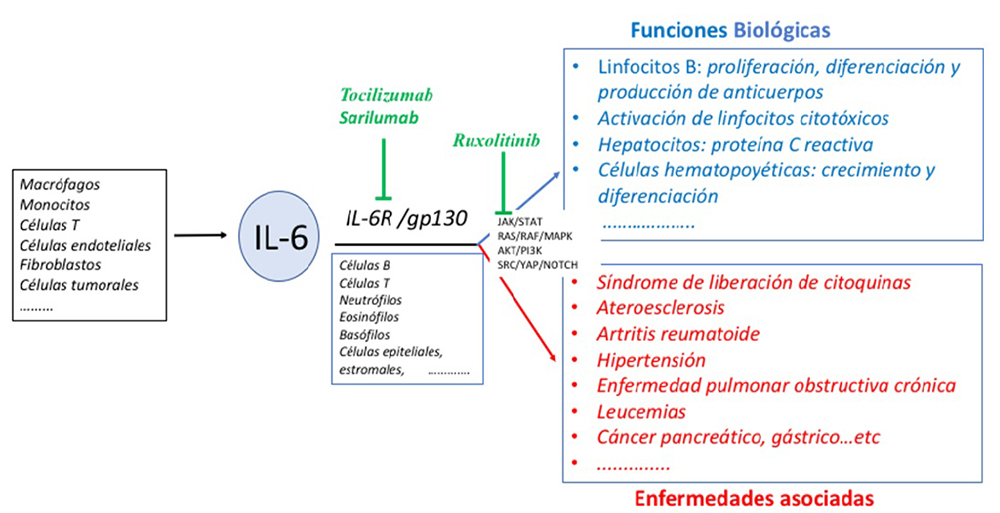
Las citoquinas son proteínas de bajo peso molecular esenciales para regular la respuesta inmune e inflamatoria. Su función es coordinar la respuesta del sistema inmunológico y lo hacen aumentando o inhibiendo las funciones de distintas células de este sistema, regulando la proliferación y diferenciación celular, activando o inhibiendo la expresión de algunos genes (incluidos genes de otras citoquinas o de sus receptores), etc. Son producidas fundamentalmente por linfocitos y macrófagos, aunque también las pueden producir otros tipos celulares. Existen muchos tipos de citoquinas, algunas con propiedades proinflamatorias y otras antiinflamatorias. De entre ellas, la IL-6 tiene un papel esencial en la respuesta inmunológica y en numerosas funciones biológicas (Figura 1). En la fase temprana de la inflamación infecciosa o no infecciosa (ej, la causada por quemaduras o lesión traumática), la IL-6 es producida por distintos tipos celulares al ser estimulados los receptores. Esta expresión aguda de IL-6 desempeña un papel central en la defensa del hospedador al estimular diversas poblaciones celulares. La IL-6 se asocia, también, con distintas enfermedades, como la artritis reumatoide, la hipertensión, ateroesclerosis, enfermedad pulmonar obstructiva crónica o distintos tipos de cáncer. Cuando la IL-6 se une a sus receptores (IL-6R, gp130) se activan vías de señalización intracelular mediadas por JAK-STAT, RAS-RAF, SRC-YAP-NOTCH o AKT-PI3K, implicadas en proliferación, diferenciación, estrés oxidativo, regulación de la respuesta inmune, etc. Cuando los niveles de IL-6 son bajos, la combinación de IL-6 con un IL-6R, anclado en la membrana (mIL-6R), conduce a la dimerización homóloga de gp130 y la señalización intracelular se limita a células del sistema inmune. Sin embargo, cuando el nivel de IL-6 aumenta, la señalización de IL-6 ocurre ampliamente porque un IL-6R soluble (sIL-6R), capaz también de unirse a gp130, puede estar en muchos tipos celulares, como las células epiteliales o estromales y provocar una respuesta inflamatoria generalizada.
Figura 1. Funciones biológicas de IL-6.
El síndrome de liberación de citoquinas (SLC) o la también llamada “tormenta de citoquinas” se produce cuando se activan gran cantidad de leucocitos (neutrófilos, macrófagos y mastocitos), lo que produce la liberación masiva de citoquinas proinflamatorias, entre ellas la IL-6, que dan lugar a una respuesta inflamatoria sistémica. Se conoce desde hace tiempo que este síndrome puede ser causado por distintos factores, como algunas infecciones víricas o algunos fármacos; también puede aparecer como complicación importante en la sepsis o enfermedades inmunológicas, como la artritis idiopática juvenil de origen sistémico, o como efecto adverso en terapias inmunológicas, como la terapia CAR-T (Chimeric Antigen Receptor T-Cell Inmunotherapy), utilizada en onco-hematología. Esta “tormenta de citoquinas” es también uno de los posibles mecanismos que puede participar en la progresión rápida y aguda de la infección por SARS-CoV-2. De hecho, se ha descrito una estrecha relación entre los casos más graves de COVID-19 y niveles circulantes elevados de IL-6 y otras citoquinas proinflamatorias y se ha sugerido que la medida de los niveles circulante de esta citoquina pueden ser un buen biomarcador que indique el pronóstico de los pacientes (3,4). Esta observación, junto con otros parámetros clínicos asociados a casos graves, como linfopenia e hiperferritinemia, ha llevado a pronosticar, que determinados pacientes sufrirán el SLC o “tormenta de citoquinas”.
Los casos graves de pacientes que sufren COVID-19 se asocian con una rápida replicación del virus y con alta tendencia de infección del tracto respiratorio. Se sugiere que el virus entraría en las células epiteliales alveolares uniéndose a la ECA2, lo que daría lugar a destrucción de las células epiteliales y aumento de la permeabilidad celular. Además, el virus activa el sistema inmune innato; los macrófagos y otras células inmunes innatas no solo capturan el virus, sino que a su consecuencia liberan una gran cantidad de citoquinas, incluida la IL-6. La inmunidad adaptativa también es activada por las células presentadoras de antígeno. Las células T y las células B no solo juegan un papel antivírico, sino que promueven también, directa o indirectamente, la secreción de citoquinas inflamatorias. Bajo la estimulación de los distintos factores inflamatorios, una gran cantidad de exudados inflamatorios y eritrocitos colmatan los alvéolos, lo que resulta en disnea e insuficiencia respiratoria (5).
Por tanto, diferentes evidencias clínicas sugieren que, en ciertos pacientes, como en personas mayores con un sistema inmune debilitado, el virus se propagaría de forma más eficaz produciendo daño tisular, liberación masiva de citoquinas proinflamatorias, hiperinflamación pulmonar y síndrome de insuficiencia respiratoria aguda, que es la principal causa de mortalidad por COVID-19. Ello ha promovido la utilización de terapias anticitoquinas y, más concretamente anti IL-6, para mitigar la hiperinflamación que ocurre en estos pacientes. Actualmente dos fármacos, Tocilizumab y Sarilumab, que bloquean los IL-6R, están sometidos a ensayos clínicos controlados, conformantes de su utilidad en los casos graves de COVID-19 asociados a niveles elevados de citoquinas.
Ensayos clínicos con bloqueantes del IL-6R
Tocilizumab (RoActemra®) es un anticuerpo monoclonal humanizado, dirigido contra el receptor de la IL-6, aprobado para el tratamiento de la artritis reumatoide. Se une específicamente tanto al receptor de membrana (mIL-6R) como al receptor soluble (sIL-6R) y así inhibe la señalización intracelular debida a la unión de Il-6 a ambos receptores. Además de su utilización en la artritis reumatoide, se emplea también en la artritis idiopática juvenil de origen sistémico, en la enfermedad de Crohn y en el tratamiento del síndrome de liberación de citoquinas, que ocurre con frecuencia con las terapias CAR-T. Se administra por vía intravenosa o subcutánea una vez por semana.
En un ensayo clínico inicial, hecho en China, con una cohorte de 21 pacientes con COVID-19 y sintomatología grave, se obtuvo una buena eficacia (6). Los 21 pacientes de COVID-19 experimentaron una rápida reducción de la fiebre, el 75 por ciento de los pacientes (15 de 20) redujeron su necesidad de oxígeno pocos días después de recibir Tocilizumab y un paciente no necesitó oxígeno tras el tratamiento. En base a estos resultados, China actualizó sus pautas de tratamiento con COVID-19 y aprobó el uso de este anticuerpo para tratar pacientes con enfermedades graves o críticas. Si bien estos datos iniciales son esperanzadores, no son concluyentes, porque se hicieron con pocos pacientes y en el ensayo no existía un grupo control, por lo que se hace necesario llevar a cabo un estudio diseñado adecuadamente, para obtener evidencia clínica sólida con respecto a la seguridad y la eficacia de Tocilizumab en el tratamiento de SARS-CoV-2. Actualmente, este fármaco está siendo utilizado en indicaciones diferentes a las autorizadas por las autoridades regulatorias, en beneficio de los pacientes, aunque sólo bajo la directa supervisión de los médicos y de acuerdo con las leyes de uso de fármacos fuera de indicación, que incluyen el consentimiento informado del paciente. Así, en distintos países, algunos centros hospitalarios lo han incluido en las pautas de tratamiento para pacientes COVID-19, ante la falta de terapias autorizadas adecuadas. Ante esta situación, la Agencia Española de Medicamentos y Productos Sanitarios ha elaborado un protocolo que regula las condiciones de uso fuera de indicación y controla la distribución de este producto.
Con el fin de disponer de evidencia científica robusta acerca de la utilidad de Tocilizumab en COVID-19, Hoffmann-La Roche ha iniciado el ensayo clínico COVACTA (7). Es un estudio multicéntrico, aleatorizado y doble ciego, que pretende evaluar la eficacia, seguridad y farmacocinética de Tocilizumab comparado con placebo, en pacientes adultos hospitalizados con neumonía grave a causa del COVID-19. Este estudio se ha iniciado a primeros de abril, incluirá 330 pacientes y están involucrados 9 países y 52 centros de todo el mundo, entre ellos seis hospitales españoles (Hospital Universitario de Bellvitge, Hospital Universitari Vall d’Hebron, Hospital Clinic de Barcelona, Hospital Universitario La Paz, Hospital Universitario Ramón y Cajal y Hospital General Universitario Gregorio Marañón). Muchos de los centros ya han empezado a reclutar pacientes y se espera que el 30 de septiembre de 2020 se haya completado el estudio. Los objetivos primarios y secundarios de este estudio de fase III incluyen la valoración del estado clínico, la mortalidad, la necesidad de ventilación mecánica y distintas variables a medir en las unidades de cuidados intensivos. Los investigadores seguirán a los pacientes durante 60 días después de la aleatorización y se realizará un análisis intermedio para buscar evidencia temprana de eficacia.
Sarilumab (Kevzara®), comercializado por Sanofi, es un anticuerpo monoclonal humano que, como Tocilizumab, se une tanto al mIL-6R como al sIL-6R e y así inhibe la señalización celular debida a la unión de Il-6 a ambos receptores. Está también autorizado para el tratamiento de la artritis reumatoide en pacientes adultos que no han respondido adecuadamente, o que son intolerantes a uno o más fármacos antirreumáticos modificadores de la enfermedad. Sarilumab se distingue de Tocilizumab, entre otros aspectos, porque tiene una vida media y una afinidad por su receptor mayor y porque se administra por vía subcutánea cada dos semanas. Con este anticuerpo se están realizando muchos ensayos clínicos, sobre todo en Estados Unidos. Uno de ellos es el ensayo CORIMUNO-SARI (8), cuyo objetivo general es determinar la eficacia y la tolerancia de Sarilumab en pacientes con neumonía asociada con COVID-19. Sarilumab se administrará a pacientes adultos hospitalizados con COVID-19 y diagnosticados de neumonía moderada o grave que no requieren ventilación mecánica o neumonía crítica que requiere ventilación mecánica. Los resultados de los pacientes tratados con Sarilumab se compararán con los de los pacientes tratados con los cuidados estándar, así como con los resultados de los pacientes tratados con otros fármacos. En total se espera la inclusión de 239 pacientes. Este estudio se llevará a cabo en siete países (Estados Unidos, Italia, Alemania, Francia, Canadá, Rusia y España) y participan en él cinco centros hospitalarios de nuestro país.
Además de los ensayos clínicos con anticuerpos que bloquean el IL-6R, se están diseñando otros ensayos encaminados a bloquear vías de señalización intracelular asociadas a la activación del IL-6R. Es el caso del ensayo clínico RUXCOVID (9), encaminado a evaluar la eficacia y seguridad de Ruxolitinib (Jakafi®), un inhibidor de la vía JAK/STAT, en pacientes graves con SLC asociada a COVID-19. Se espera la inclusión de 64 pacientes. Ruxolitinib se utiliza en pacientes con policitemia vera, que son resistentes o intolerantes a la hidroxiurea. Dada la rápida propagación de la pandemia, y mientras se finalizan el diseño el estudio, Novartis también ha establecido un programa internacional de uso compasivo para determinados pacientes y siempre sujeto a las regulaciones de los países.
En resumen, en estos pocos meses que llevamos de pandemia, la intensa actividad investigadora, que se está realizando ha podido demostrar que el SARS-CoV-2 provoca una “tormenta de citoquinas” en algunos pacientes, que se asocia con la gravedad y mortalidad de la enfermedad. Comprender la alteración de la respuesta inmune en pacientes con COVID-19, no sólo proporciona una mayor comprensión de la patogénesis del SARS-CoV-2, sino que también identifica nuevas dianas para el tratamiento de estos pacientes. Actualmente se están utilizando distintos fármacos antivíricos, pero el uso de estos fármacos por sí solos, puede llegar tarde si se administran cuando la “tormenta de citoquinas”, a la que se ven sometidos algunos pacientes, está ya en marcha. La utilización de fármacos dirigida a reducir la acción de distintas citoquinas podría mejorar la inflamación pulmonar, la dificultad respiratoria y la mortalidad. Además, los estudios que investigan los componentes víricos, que ocasionan esta alteración del sistema inmune, pueden proporcionar información sobre cómo obtener una vacuna que proporcione la deseada inmunidad protectora.
Referencias
1. Avendaño C. Aportaciones de las ciencias biomédicas en el estado de alarma motivado por la pandemia del virus SARS-COV-2. An Real Acad Farm. 2020. 86: 09-17
2. Ministerio de Sanidad, Consumo y Bienestar Social-Centro de Coordinación de Alertas y Emergencias Sanitarias. Enfermedad por coronavirus, COVID-19. https://www.mscbs.gob.es/profesionales/saludPublica/ccayes/alertasActual/nCov-China/documentos/20200404_ITCoronavirus.pdf. 04.04.2020
3. Chen X, Zhao B, Qu Y, et al. Detectable serum SARS-CoV-2 viral load (RNAaemia) is closely associated with drastically elevated interleukin 6 (IL-6) level in critically ill COVID-19 patients. bioRxiv. 2020
4. Ulhaq ZS, Soraya GV. Interleukin-6 as a potential biomarker of COVID-19 progression. Med Mal Infect. 2020 Apr 4 doi: 10.1016/j.medmal.2020.04.002 [Epub ahead of print]
5. Chi Zhang, Zhao Wu, Jia-WenLi, et al. The cytokine release syndrome (CRS) of severe COVID-19 and Interleukin-6 receptor (IL-6R) antagonist Tocilizumab may be the key to reduce the mortality. Int J Antimicrob Agents. 2020 Mar 29: 105954. doi: 10.1016/j.ijantimicag.2020.105954 [Epub ahead of print]
6. Xiaoling Xu, Mingfeng Han, Tiantian Li, et al., Effective Treatment of Severe COVID-19 Patients with Tocilizumab. http://chinaxiv.org/abs/202003.00026
7. A Randomized, Double-Blind, Placebo-Controlled, Multicenter Study to Evaluate the Safety and Efficacy of Tocilizumab in Patients With Severe COVID-19 Pneumonia (COVACTA). (ClinicalTrials.gov Identifier: NCT04320615)
8. Cohort Multiple Randomized Controlled Trials Open-label of Immune Modulatory Drugs and Other Treatments in COVID-19 Patients-Sarilumab Trial – CORIMUNO-19 – SARI (CORIMUNO-SARI) (ClinicalTrials.gov Identifier: NCT04324073)
9. Study of the Efficacy and Safety of Ruxolitinib to Treat COVID-19 Pneumonia (ClinicalTrials.gov Identifier: NCT04331665)
Mercedes Salaices
Académica de la RANF