Tipos de programas de creación de vacunas contra el SARS-CoV-2
Vacunas Desarrollos
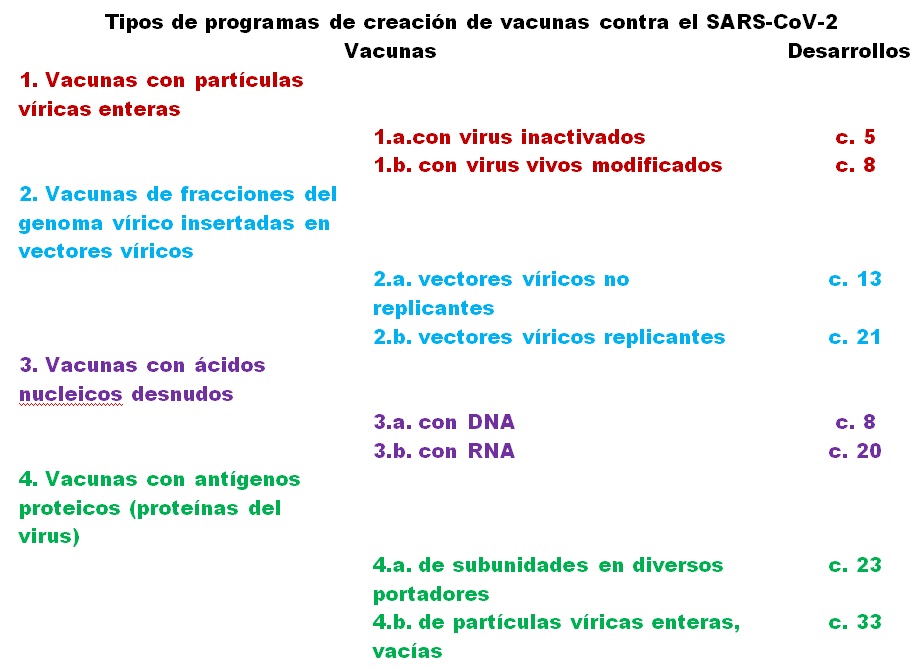
El primer campo, vacunas de partículas víricas completas, es el más clásico. Las dos variedades de la tabla cuentan, a su vez, con variaciones que elaboran productos bien diferentes; las 1.a. inactivadas están formadas por partículas víricas ‘muertas’, con o sin adyuvantes, inactivadas por la acción de aldehídos, calor, etc.; las 1.b. son mucho más elaboradas, se producen con virus atenuados por diferentes métodos: clásicamente por pases reiterados por infección de embriones filogénicamente alejados, cultivos celulares o animales vivos de experimentación; actualmente se obtienen por modificación del genoma mediante técnicas de manipulación incluida la edición, dirigidas a disminuir su patogenicidad, o anularla, conservando su inmunogenicidad protectora frente a la infección por cepas salvajes del virus.
El bloque 2 resume las vacunas producidas mediante vectores víricos; son virus modificados, apatógenos, capaces de penetrar en las células presentadoras, que portan en su genoma, insertados a propósito, los genes que expresan proteínas constitutivas de las espículas y/o de la cápside del coronavirus. En las variantes 2.a, con amplia experiencia práctica en la terapia génica, el virus portador carece de capacidad de reproducirse; se utilizan como portadores adenovirus heterólogos, de simios por ejemplo, o poxvirus como el Ankara modificado; la antigenicidad de estas vacunas puede requerir la aplicación de inoculaciones de recuerdo. Las variantes 2.b utilizan como portadores virus homólogos atenuados; los virus portadores infectan y se reproducen a la par que, por ello, informan mucho más ampliamente al sistema inmune, un portador típico de estas vacunas es el virus atenuado del sarampión, un inconveniente de su uso es la inmunidad residual infecciosa o vacunal frente al sarampión, la vacuna así formada protegerá a los que ya no tengan memoria inmune frente al sarampión.
El bloque 3 lo forman las vacunas de ácidos nucleicos. DNA complementario del RNA vírico o RNA que serán aplicados directamente o transportados por un sistema vectorial. En las vacunas 3.a los genes de las espículas del coronavirus, incorporados a un plásmido, son inyectados directamente por electroporación, inyección que crea poros forzados en las células a través de los cuales se incorpora el plásmido transportador; llevado al núcleo por las trasnportinas, se producen los RNA mensajero capaces de sintetizar las proteínas del virus inductoras de la respuesta humoral y celular. En las vacunas 3.b el RNA, desnudo de los genes de las espículas u otros, van encapsulado en un liposoma, que le incorpora directamente al citoplasma; comportándose como un mensajero se traduce en las proteínas antigénicas, inductoras de la respuesta inmune.
El bloque 4 lo forman las vacunas aparentemente más seguras. Las 4.a son vacunas de subunidades proteicas (antigénicas del virus) particularmente de las espículas o de aquellas fracciones moleculares clave en la asociación receptor/ligando para la penetración del virus; estas vacunas de componentes, de partes diseccionadas del virus, producidas masivamente en una plataforma de Pichia sp. u otra levadura, se inoculan mezcladas con adyuvantes, es decir, moléculas inmunoestimulantes; las vacunas de esta clase necesitan frecuentemente aplicaciones de recuerdo para crear una inmunidad alta y duradera (vacunar y revacunar), lo que es en sí un inconveniente. Las 4.b son un poco más sofisticadas; en este caso se imita la antigenicidad que la superficie total del virus puede ocasionar; los genes totales que expresan las espículas del virus van incorporadas en partículas VLPs (como partículas víricas) vacías, sin genoma; son eficacísimas en la inducción de una respuesta inmunitaria sólida, hay varias vacunas licenciadas en el mercado con esta tecnología, frente a otros agentes patógenos. Unos cinco centros diferentes trabajan en la actualidad en la puesta a punto de una vacuna de este tipo.
También están afanados en esta tarea centros españoles con plataformas capaces de crear vacunas en los campos 1.b y 2.a, además cuentan con experiencia y medios las dos ICTS (Infraestructuras Científica y Técnica Singulares), INIA-CISA en Madrid e IRTA-CReSA en Barcelona.
Antonio R. Martínez Fernández
Académico secretario de la RANF


