Page 78 - girbes
P. 78
niveles, el celular, sobre las células tumorales y el vascular, sobre la
neovasculatura tumoral. Como se observa en la figura 20, la destrucción de
unas pocas células endoteliales destruye el vaso y provoca la liberación de
la inmunotoxina, que pueden entonces actuar también sobre las células
cancerosas CD105+y sobre las células endoteliales destruyendo los vasos y
provocando la necrosis del tumor por falta de oxígeno y nutrientes. Por
ello, las inmunotoxinas nigrina b-MJ7 son antiangiogenicas.
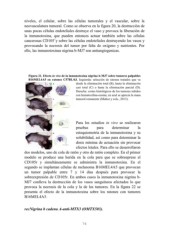
Figura 21. Efecto in vivo de la inmunotoxina nigrina b-MJ7 sobre tumores palpables
B16MEL4A5 en ratones C57BL/6J. Izquierda: selección de ratones tratados que va
desde la eliminación total (B), hasta la eliminación
casi total (C) o hasta la eliminación parcial (D).
Derecha: cortes histológicos de los tumores teñidos
con hematoxilina-eosina; en azul se aprecia la masa
tumoral remanente (Muñoz y cols., 2013).
Para los estudios in vivo se realizaron
pruebas para determinar la
estequiometría de la inmunotoxina y su
solubilidad, así como para determinar la
dosis mínima de actuación sin provocar
efectos letales. Para ello se desarrollaron
dos modelos, uno de cola de ratón y otro de ratón completo. En el primer
modelo se produce una herida en la cola para que se sobreeprese el
CD105r y simultáneamente se administra la inmunotoxina. En el
segundo se implantan células de melanoma B16MEL4A5 que provocan
un tumor palpable entre 7 y 14 dias después para provocar la
sobreexpresión de CD105r. En ambos casos la inmunotoxina nigrina b-
MJ7 conlleva la destrucción de los vasos sanguíneos afectados lo que
provoca la necrosis de la cola y la de los tumores. En la figura 22 se
presenta el efecto de la inmunotoxina sobre los ratones con tumores
B16MEL4A5.
recNigrina b cadena A-anti-MTX3 (OMTX503).
76